
EXPERIMENTAL THERAPEUTIC TRANSPLANTATION OF EMBRYONIC STEM CELL DERIVED RETINAL PIGMENT EPITHELIAL CELLS IN ANIMAL MODELS FOR RETINAL DEGENERATION
Prof dr AAB Bergen, Academisch Medisch Centrum, AmsterdamHet retina pigment epitheel (RPE) is een cellaag in het achterste deel van het oog welke betrokken is bij vele (genetische bepaalde) netvlies-ziekten, waaronder leeftijdsgebonden macula degeneratie (OMD) en sommige vormen van retinitis pigmentosa.
Therapeutisch embryonaal stamcel (ES) onderzoek aan het RPE leverde recent veelbelovende resultaten op: Zo werd, in het laboratorium, uit ES-cellen RPE-achtige cellen gekweekt, die succesvol werden teruggeplaatst in diermodellen met een dysfunctionerend RPE. Ook werd recent de eerste op stamcel gebaseerde clinical trial, in 2 patiënten met OMD en de ziekte van Stargardt, goedgekeurd door de Amerikaanse FDA.
In Nederland werd 2 jaar geleden, op initiatief van de huidige subsidie aanvrager, begonnen met therapeutisch gericht retinaal stamcel onderzoek. Het huidige, nu lopende onderzoek richt zich op 2 zaken: Het maken van pluripotentie ES cellen uit huidcellen, en het verder verbeteren van de kweek en differentiatie protocollen voor RPE ES cellen. Het toekomstig therapeutisch doel is: Afname van een huidbiopt bij een patiënt (met een oogziekte), verandering van deze huidcel in een pluripotente ES cell, en vervolgens verandering van deze pluripotente ES cell in een RPE cell die vervolgens gebruikt kan worden voor transplantatie en uiteindelijk herstel van gezichtsvermogen.
Onze resultaten zijn tot nu toe boven verwachting: Zo zijn we inmiddels in staat om in ons laboratorium uit (pluripotente) embryonale stamcellen volledig gedifferentieerde RPE cellen te kweken. Wij kunnen deze RPE ES cellen in Nederland verder uitstekend moleculair karakteriseren, wat de slagingspercentages (%) bij toekomstige experimentele therapie/terugplaatsing sterk zal verbeteren. Daar wij inmiddels, zowel bij mens en diermodel (muis) de moleculaire machinerie (genexpressie profielen) van het RPE, photoreceptors en choroid kennen, zijn we nu klaar voor experimentele therapie; dwz terugplaatsing van RPE ES cellen in diermodellen voor retinale degeneratie. Het nu lopende onderzoek resulteert de komende jaren meerdere malen, steeds verbeterde, RPE ES cellen. Of die RPE ES cellen ook daadwerkelijk beter functioneren en dus geschikt zijn voor (experimentele) therapie moet noodzakelijkerwijs worden getest in diermodellen:
Wij stellen dan ook, naast het nu reeds lopende onderzoek aan de kweek en differentiatie methoden, het volgende nieuwe onderzoek voor:
Gedifferentieerde en gekarakteriseerde RPE ES cellen zullen (a) worden gedissocieerd en via subretinale injectie worden teruggeplaatst, en (b) gekweekt worden op een artificieel Bruch´s membraam en worden teruggeplaatst, beide in de retina van muis modellen met RPE degeneratie. Het effect en therapeutisch succes van terugplaatsing zal worden gemonitoord met diverse oogheelkundige, histologische en functionele onderzoeks technieken (funduscopie, SLO, OCT). De beste RPE ES cellen en transplantatie protocollen zullen worden geselecteerd voor verder onderzoek en/of ter voorbereiding van clinical trials.
(in Nederland).
REGULATION OF INFLAMMATION BY BAP1
Dr. M.J. Jager, Leids Universitair Medisch Centrum
Ontstekingen spelen bij veel ziekten, waaronder bloedvatverkalking en leeftijdsgebonden aandoeningen van het netvlies en oogkanker, een belangrijke rol. Kenmerken van ontsteking zijn de aanwezigheid van een bepaald type witte bloedcellen, macrofagen genoemd, en van ontstekingsmediatoren. De productie van deze ontstekingsfactoren door cellen vindt plaats nadat binnen een cel een cascade van eiwitinteracties gestart wordt die uiteindelijk leidt tot activering van een eiwitcomplex, NFkB genoemd. NFkB activering leidt tot de uiteindelijke transcriptie van het cellulaire DNA dat codeert voor allerlei ontstekingsfactoren. Om deze cascade van eiwitinteracties gecontroleerd te laten verlopen bestaan er binnen de cel allerlei eiwitten die dit reguleren.
Bij het bestuderen van oogkanker zagen wij dat speciaal die oogkankers waarbij vaak uitzaaiingen optreden, macrofagen bevatten. Dezelfde oogkankers blijken een functioneel verlies te tonen van een eiwit genaamd BAP1, ook wel bekend onder de naam UCHL2 en lid van de familie van UCH-eiwitten. Een ander familielid van dit type eiwitten is UCHL1, welke een belangrijke rol speelt bij het voorkomen van ontstekingen in bloedvaten en huidcellen doordat het de NF-kB activering kan onderdrukken. Omdat wij een sterke relatie zien tussen verlies van BAP1 en het optreden van ontstekingsinfiltraat in oogkanker denken wij dat BAP1/UCHL2, net zoals UCHL1, een belangrijke onderdrukker is van ontstekingen. Het zou zo maar kunnen dat verlies van BAP1 leidt tot activering van NFkB en daardoor tot productie van allerlei ontstekingsmediatoren die macrofagen aantrekken.
Via een eerste serie experimenten in het laboratorium hebben we aanwijzingen gekregen die deze hypothese lijken te bevestigen. Wij willen deze hypothese verder bestuderen door te onderzoeken of de eerder door ons gevonden relatie tussen verlies van BAP1 expressie en de aanwezigheid van een ontstekingsinfiltraat geassocieerd is met activering van de NFkB. Onder bepaalde omstandigheden, welke vaak voorkomen bij kankers, kan NF-kB activering plaatsvinden. Wij willen onderzoeken wat dit voor effect heeft op de productie van ontstekingsfactoren. Om na te gaan hoe BAP1 deze processen reguleert, zullen de verschillende functies die BAP1 zou kunnen uitvoeren worden geblokkeerd waarna de effecten op de productie van ontstekingsmediatoren in kaart worden gebracht. Tenslotte zullen we in twee diermodellen voor oogkanker (muis en zebravis) bestuderen wat het effect van uit- of aanschakelen van BAP1 is op de aantrekking van ontstekingscellen alsook wat de invloed hiervan is op bestaande en experimentele behandelingen van oogkanker (in de muis). Deze studies moeten laten zien of BAP1 een belangrijke regulator is van ontstekingsreacties. Indien dit zo is, kan het zijn dat BAP1 ook een regulator is van ontstekingsreacties bij andere leeftijdsgebonden aandoeningen in het oog.
Prime suspect: AUTOIMMUNITY IN CHORIORETINAL DISORDERS
Prof.dr A. Rothova, Universitair Medisch Centrum Utrecht
Onze studie heeft als doel om de laboratoriumtechnieken in Nederland te ontwikkelen die nodig zijn voor het meten van diverse antistoffen gericht tegen ons netvlies en vaatvlies in bloed en in oogvloeistof en het belang van deze antistoffen te onderzoeken bij diverse chorioretinale aandoeningen.
Ons afweersysteem kan onder bepaalde omstandigheden zgn. auto-antistoffen produceren die gericht zijn tegen ons eigen netvlies. In dat geval is sprake van een auto-immuun retinopathie (AIR), welke schade aan het netvlies en uiteindelijk blindheid kan veroorzaken. Een dergelijk fenomeen is betrokken bij diverse ernstige oogafwijkingen, waaronder bijvoorbeeld “cancer-associated retinopathy” en “melanoma-associated retinopathy”. De activiteit van ons afweersysteem kan onderzocht worden door deze anti-retinale antistoffen (ARA’s) te meten in het laboratorium. Helaas bestaat er momenteel in Nederland geen mogelijkheid om ARA’s te meten. Indien gewenst, wordt bloed voor dit doeleinde naar Duitsland gestuurd, alwaar een laboratorium in staat in om een tweetal ARA’s te meten.
ARA’s zijn ook gevonden bij patiënten met leeftijdsgebonden maculadegeneratie (AMD), dat gezien de toenemende vergrijzing een steeds prominentere rol speelt bij het ontstaan van slechtziendheid en blindheid. Recent is gebleken dat de niveaus van ARA’s in bloed samenhangen met de activiteit van de AMD. Ook zijn ARA’s gevonden bij diverse ontstekingen, bij erfelijke netvliesaandoeningen zoals retinitis pigmentosa en bij oogafwijkingen door suikerziekte. De precieze rol van ARA’s bij de diverse retinale aandoeningen is vooralsnog onbekend en men heeft diverse theorieën ontwikkeld over hun mogelijke rol. Onze hypothese is dat door het ontstaan van de ARA’s, er bij diverse retinale aandoeningen zoals bijv. maculadegeneratie een milde ontsteking ontstaat, die het ziektebeloop nadelig beïnvloedt (zoals het chronisch of progressief worden van de oogziekte). Indien onze hypothese klopt, zullen de resultaten van onze studie van grote betekenis zijn voor de patiënten met diverse chorioretinale aandoeningen, omdat het remmen (of voorkomen) van de ontsteking het ziektebeloop gunstig kan beïnvloeden.
Wij willen de benodigde laboratoriumtechnieken voor het meten van ARA’s in bloed en oogvloeistof ontwikkelen in het gecertificeerde immuno-diagnostisch laboratorium van het Erasmus MC te Rotterdam. Gezien de reeds opgebouwde expertise en ervaring van het laboratorium bij andere auto-immune aandoeningen lijkt het ons een geschikte keuze en voorzien wij een grote kans van slagen. Ons plan is om als eerste het meten van ARA’s in bloed in Nederland mogelijk te maken, hetgeen een vroege diagnose van AIR in Nederland mogelijk kan maken. In de daarop volgende fase, zullen wij de technieken gebruiken om de diverse ARA’s in het bloed en intra-oculaire vloeistof te bepalen en hun rol vaststellen bij het ontstaan en chronisch worden van de diverse chorioretinale aandoeningen met inbegrip van AMD.
COLLAGEN CROSS-LINKING BY NEAR INFRARED ILLUMINATION (NIR) OF BACTERIOCHLOROPHYLL DERIVATIVES FOR THE TREATMENT OF KERATOCONUS AND CORNEAL ECTASIA: SAFETY, EFFICACY AND MECHANISMS OF ACTION
Dr R.M.M.A. Nuyts, Maasticht Universitair Medisch Centrum
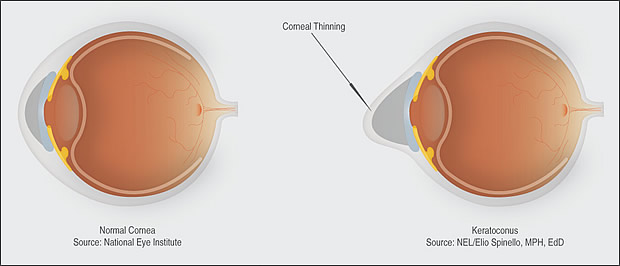
Keratoconus is de meest voorkomende degeneratieve aandoening van het hoornvlies, voorkomend bij ongeveer 1 op 1000 personen.1 Naar schatting lijden 16.000 personen in Nederland aan deze ziekte. Bij keratoconus verandert het hoornvlies van structuur, verliest het zijn kracht en wordt dunner.2 Hierdoor vervormt het hoornvlies en worden lichtstralen op een foutieve manier gebroken. De aandoening presenteert zich meestal tijdens de puberteit, en kent een progressie met mogelijk desastreuze gevolgen voor het zicht en daarnaast enorme sociale en economische gevolgen. De huidige behandelingen bestaan uit correctie met contactlenzen in het beginstadium, verstevigen van het hoornvlies via cross-linking in progressieve gevallen, implantatie van ringen in het hoornvlies en in de meest gevorderde gevallen gedeeltelijke of volledige vervanging van het hoornvlies met die van een donor.
Cross-linking
Bij cross-linking wordt een lichtgevoelige vloeistof (riboflavine A; RF) op het hoornvlies aangebracht, waarna het wordt beschenen met ultraviolet-A licht (UVA). De lokale reactie die hierbij ontstaat, zorgt voor versteviging van het hoornvlies waarmee getracht wordt de verdunning en vormverandering te vertragen. Echter, het gebruikte UVA licht is schadelijk voor zowel de patiënt als de operateur en de procedure is erg tijdsintensief.3 Daarbij kan de behandeling niet worden toegepast als het hoornvlies te dun is zoals juist bij vergevorderde patiënten het geval is. Tevens is de behandeling niet altijd effectief en moet de buitenste laag van het hoornvlies (het epitheel) verwijderd worden met pijn en een vertraagd herstel als gevolg.
De voorlopige resultaten uit proefdierstudies van onze onderzoeksgroep laten zien dat de onschadelijke stof WST11 in combinatie met nabij infrarood licht (NIR) evenveel effect heeft op de versteviging van het hoornvlies als RF/UVA.4 De bijkomende voordelen van deze techniek daarentegen zijn dat dit licht niet schadelijk is voor patiënt of operateur, hiermee ook vergevorderde patiënten behandeld kunnen worden en dat het epitheel niet verwijderd hoeft te worden. Studies met menselijk donor weefsel, om de veiligheid en effectiviteit van deze behandeling vast te stellen, zijn tot op heden nog niet uitgevoerd. Tevens zijn er nog steeds onduidelijkheden over het werkingsmechanisme van WST11/NIR in de behandeling van keratoconus.
Doelen
- Het bepalen van de veiligheid en effectiviteit van WST11/NIR.
- Het vaststellen van de optimale dosering, behandelduur en lichtintensiteit om een gestandaardiseerd behandelprotocol te formuleren.
- Het achterhalen van de mechanismen waarmee WST11/NIR het hoornvlies kan verstevigen.
Om deze doelen te bereiken is er een internationale studiegroep gevormd, bestaande uit specialisten op zowel klinisch als fundamenteel niveau, van de volgende instituten:
- Universiteitskliniek voor Oogheelkunde, Maastricht, Nederland
- Weizmann Institute of Science, Rohovot, Israël
- Maastricht University, Maastricht, Nederland
- Technische Universiteit Eindhoven, Eindhoven, Nederland
- Euro Cornea Bank, Beverwijk, Nederland
GENETICS IN GLAUCOMA PATIENTS FROM AFRICAN DESCENT. THE GIGA STUDY.
Dr A.A.H. J. Thiadens, Erasmus Medisch Centrum Rotterdam
Glaucoom is een belangrijke oorzaak van blindheid wereldwijd. De ziekte kenmerkt zich door schade en verlies van zenuwvezels in de oogzenuw en uitval van het gezichtsveld. In een vergevorderd stadium kan glaucoom leiden tot blindheid. De meest voorkomende vorm van glaucoom is primair open-kamerhoek glaucoom (POAG). De oogdruk is de belangrijkste risicofactor voor POAG. Het reguleren van de oogdruk is op dit moment de enige therapie, maar helaas is dit niet altijd effectief. Er bestaat dus een klinische vraag naar nieuwe behandelingsmogelijkheden voor POAG.
De oorzaken van POAG zijn nog grotendeels onbekend. Naast hoge oogdruk zijn er andere risicofactoren voor POAG, zoals hoge leeftijd, familiare belasting, Afrikaanse afkomst en hoge bijziendheid. Het afgelopen decennium is veel belangstelling ontstaan voor de genetische achtergrond van POAG. Nieuwe geavanceerde technieken zoals een zgn ‘genoomscan’ hebben het mogelijk gemaakt nieuwe genen te vinden. Onze studies in Rotterdam hebben hieraan een belangrijke bijdrage geleverd. Toch verklaren deze genen tezamen maar een klein deel van de ziekte. Er moeten dus nog veel meer genetische factoren zijn die vooralsnog niet ontdekt zijn.
Het onderzoek naar de erfelijkheid van POAG heeft zich tot op heden gericht op Europese en Aziatische populaties. Echter, POAG komt bij personen van Afrikaanse afkomst ~5 keer zo vaak voor. Ook hebben Afrikaanse patiënten vaak een agressiever beloop van de ziekte met een hogere kans op blindheid. Deze factoren maken het waarschijnlijk dat genetisch onderzoek bij Afrikanen meer genetische risicofactoren voor POAG zal opleveren dan bij Europeanen of Aziaten het geval is.
In 2012 is een samenwerking ontstaan tussen twee ziekenhuizen in Tanzania en het Erasmus MC. De samenwerking kwam tot stand nadat de onderzoeksleider de kans kreeg om een tijd als oogarts te werken in één van deze Afrikaanse ziekenhuizen. Het aantal POAG patiënten bleek opvallend hoog te zijn. Een pilot project werd gestart met Rotterdamse geneeskunde studenten om te zien of het logistiek mogelijk was om Afrikaanse patiënten uit Tanzania te includeren in een genetisch epidemiologische studie. Dit pilot project liep bijzonder goed: inmiddels zijn er 389 personen geïncludeerd en is hun DNA opgeslagen in het Erasmus MC. Een tweede pilot studie werd gestart met het Groote Schuur Ziekenhuis in Kaapstad, Zuid-Afrika, en ook dit project was bijzonder succesvol. Deze pilot studies hebben de weg gebaand voor het ontwerpen van een grote studie.
In deze aanvraag vragen wij financiële middelen voor het includeren en verzamelen van DNA van 1000 Afrikaanse glaucoom patiënten en 1000 controle personen. Wij zullen de patiënten in Tanzania en Zuid-Afrika uitgebreid oogheelkundig onderzoeken, een vragenlijst afnemen voor risicofactoren en bloed afnemen voor DNA. Wij zullen deze patiënten vergelijken met onze Nederlandse glaucoom patiënten en onderzoeken of de bekende genetische factoren hetzelfde zijn. Uiteindelijk zullen we andere studies met Afrikaanse glaucoom patiënten vragen om met ons een consortium te vormen voor het vinden van nieuwe genen voor glaucoom. Wij verwachten dat onze studieresultaten zullen bijdragen aan het vinden van oorzaken van glaucoom met nieuwe startpunten voor behandeling.
IDENTIFICATION OF NOVEL HUMAN RETINAL DYSTROPHY GENES BY SEQUENCE ANALYSIS OF GENES MUTATED IN MAMMALIAN MODELS WITH VISUAL IMPAIRMENT
Anna M. Siemiatkowska, Radboud Medisch Centrum Nijmegen
Personen met netvlies degeneratie vertonen gezichtsveldbeperkingen die vaak tot volledige blindheid kunnen leiden. Deze groep van aandoeningen omvat een groot aantal verschillende klinische beelden, die o.a. van elkaar onderscheiden kunnen worden op grond van de leeftijd waarop de eerste symptomen optreden, de mate van progressie, en de initiële betrokkenheid van kegeltjes of staafjes. Het betreft met name de volgende netvliesziekten: kegel en kegelstaaf dystrofie (cone dystrophy -CD; cone-rod dystrophy - CRD), aangeboren blindheid (Leber’s congenitale amaurose - LCA), en retinitis pigmentosa (RP). Genetische defecten zijn nog niet gevonden bij ongeveer 30% van personen met LCA, 40% van de RP patiënten, en 60% van CD/CRD families. Deze onbekende oorzaken omvatten mutaties in reeds bekende ziektegenen die wij niet kunnen opsporen met conventionele methodes, maar zullen zeker ook mutaties in nieuwe ziektegenen omvatten.
Vrijwel alle genen die betrokken zijn bij netvlies degeneratie zijn gemuteerd bij enkel 1% van de aangedane personen. Voor het identificeren van nieuwe oorzakelijke genen moet er daarom worden voldaan aan twee belangrijke voorwaarden. We moeten de beschikking hebben over een zeer groot aantal patiënten en een kosteneffectieve DNA sequentie analyse methode.
Aan de eerste voorwaarde konden wij reeds voldoen. Door onze patiëntengroepen te combineren met die van 11 andere Europese groepen hebben we de beschikking over het genetische materiaal van circa 10.000 families met netvliesziekten, en konden wij in de afgelopen jaren 7 nieuwe oorzakelijke genen en twee nieuwe genotype-fenotype associaties vinden.
Daarnaast hebben in de afgelopen jaren relatief goedkope (€1500/patiënt), grootschalige DNA sequentie analyses methodes het vinden van nieuwe ziektegenen gefaciliteerd. Exome sequentie analyse, waarbij de eiwitcoderende onderdelen van het DNA (de exonen) van alle 22.000 humane genen worden geanalyseerd, is de meest gebruikte methode. Recent werd een kosteneffectieve (€100/patiënt) techniek ontwikkeld waarin maximaal 100 genen geanalyseerd kunnen worden in grote aantallen patiënten (de zogenaamde molecular inversion probe – MIP strategie), met zeer lage reagentia kosten van slechts 1€ per persoon per gen.
Veel van 100 genen die betrokken zijn bij niet-syndromale erfelijke netvliesziekten van de mens, werden gevonden door de analyse van genen die gemuteerd zijn bij zoogdieren met erfelijke netvliesziekten (b.v. NRL, PRCD, RBP3). Veel andere genen werden als kandidaatgenen beschouwd vanwege hun retinaspecifieke functies. Omdat er nog diverse andere zoogdiermodellen zijn met netvliesdegeneratie met mutaties in genen die nog niet geassocieerd zijn met erfelijke netvliesziekten bij de mens, veronderstel ik dat ook IRD patiënten mutaties in deze genen zullen dragen. Het is mijn doel om deze oorzakelijke varianten in dit soort genen op te sporen, die als basis kunnen dienen om aansluitend de moleculaire mechanismen van de geassocieerde ziekten te kunnen bestuderen.
In dit projectvoorstel vraag ik financiering voor een 1,5-jaar durende studie waarin ik 20 kandidaatgenen wil testen op mutaties in 1.000 patiënten met erfelijke netvliesziekten. Ik denk dat deze studie zal resulteren in 5 nieuwe genen die betrokken zijn bij erfelijke netvliesziekten. Deze bevindingen zullen niet alleen de erfelijkheidsadvisering verbeteren, maar ook nieuwe inzichten geven in ziekte mechanismen, en daardoor op de lange termijn een basis vormen voor het ontwikkelen van nieuwe therapieën.
| Copyright © 2024 ANVVB All rights reserved. |
| ||
